nCounterユーザーインタビュー
順天堂大学医学部 人体病理病態学 准教授 齋藤剛 先生に、がん個別化医療を目指したご研究やnCounter®でのimbalance解析を用いた融合遺伝子スクリーニングについて伺いました。
がん治療に直結する臨床研究と発症メカニズム解明の二本柱で、研究を進めていきます。

順天堂大学 医学部 人体病理病態学
准教授 齋藤 剛 先生
治療に直結し、患者様に還元できる研究を常に心がけています。
―2020年に報告された平滑筋肉腫 でのチロシンキナーゼ融合遺伝子(MAN1A1/ROS1融合遺伝子)の発見1や、高悪性軟部肉腫でのGLI1遺伝子のコピー数異常と薬剤効果のご研究2など、レアながんでの個別化医療にアプローチをされている印象がございますが、理由や背景などをお伺いできますか?
臨床検体は臨床各科からご提供いただいていますが、私はもともと整形外科医で、その後大学院進学で病理学を選択しました。そのため肉腫を中心としたがんの研究を行っており、現在はより幅広いがん種を扱っています。骨や筋肉などに起こる肉腫は、日本人が罹患するがんの中でも1%程度の稀ながんのため、薬剤開発が進んでいません。基礎研究も大事だとは思っていますが、治療に直結するような、患者様に還元できる研究を常に心がけています。
―平滑筋肉腫 でのチロシンキナーゼ融合遺伝子の先生の発見は、臨床的にどのような意義を与えたのでしょうか?
歴史的には、融合遺伝子は1990年代頃から悪性リンパ腫や白血病で報告されるようになり、今やそれを標的にした分子標的薬が開発されています。肉腫でも、次第に腫瘍特異的な融合遺伝子が報告されるようになり、その有無が診断マーカーとして利用されるようになりましたが、残念ながら治療標的となるような融合遺伝子は見つかっていませんでした。今回の平滑筋肉腫での新規融合遺伝子の発見は、発がん因子として診断だけでなく、肺がんの抗がん剤として用いられるクリゾチニブが、肉腫でも有効である可能性が分かったことに、意義があると思っています。
日本でも2019年からがん遺伝子パネル検査が保険適用され、順天堂医院も連携病院となっています。医薬品の適応判定の補助を目的として、DNAの変異だけでなく一部の融合遺伝子も適用されています。順天堂医院は、それに先駆けて2016年から世界最高精度のがんクリニカルシークエンス検査(MSK-IMPACT)を導入しており、468個にのぼるがん関連遺伝子のDNAパネルによる遺伝子変化の解析とRNAパネルによるトランスクリプトームレベルでの補助的検査をスタートしていました。今回、 NanoString nCounterを用いることでトランスクリプトーム解析の有用性が確認できたため、今後もRNAベースの解析を重ねることで、希少がん軟部肉腫における一歩進んだ個別化医療の展開に協力できるように努力していきます。
nCounterによるimbalance解析3は融合遺伝子のスクリーニングに適した手法だと思います。
―チロシンキナーゼ融合遺伝子のご研究では、弊社 nCounter®でのカスタムパネルを用いたimbalance解析をご利用いただきありがとうございます。融合遺伝子検出手法としてnCounterを選択いただいた理由をお伺いできますか?
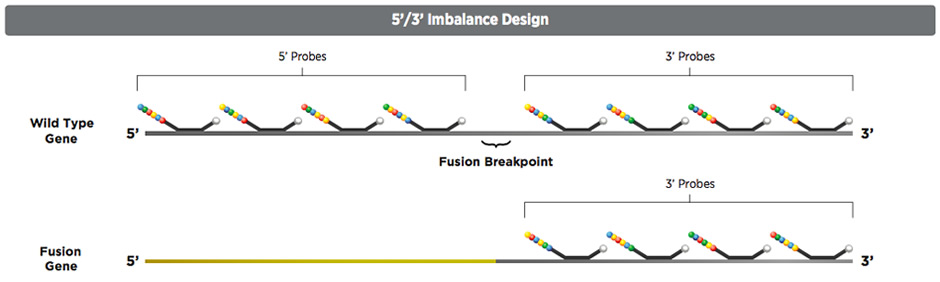
融合遺伝子を見つけるストラテジーはさまざまありますが、今最もポピュラーなのがNGSだと思います。NGSの解析コストは飛躍的に安くなっていますが、まだ多くの検体を解析するにはそれなりに費用がかかります。今回私が選択したNanoStringのimbalance 解析は、チロシンキナーゼ受容体遺伝子を多数含むパネルを用いていますが、融合遺伝子を含むものを網羅的に見つけていくようなアッセイではなく、とりあえず何かしらの融合遺伝子を有する確率が高いと想定することが出来るようなアッセイなので、スクリーニングに適しています。
平滑筋肉腫で見つけた1例は、imbalance解析で陽性となったサンプルですが、これはその時点では本当に融合遺伝子があるのか、融合遺伝子パートナーが何かもわかりません。多数の検体で統計解析を行うと、5’と3’の発現値が異なる(imbalance解析)検体が発見できたときに、ピックアップして最後にNGSにかけて配列を確認し、平滑筋肉腫で治療対象となる新規チロシンキナーゼ融合遺伝子を同定しました。この研究はがんセンターとの共同研究でしたので、NGSによる解析はがんセンターの共同研究(間野博行先生・高阪真路先生)の先生方にお願いしました。
―imbalance解析は新規融合遺伝子を発見できる可能性があり、コスト面で優れているということでしょうか?
今回のチロシンキナーゼはたまたま新規でしたが、nCounterでのimbalance解析は、融合遺伝子があるかどうかをスクリーニングするのに、リーズナブルな方法ではないかと思っています。融合遺伝子の検出手法には色々あり、診断分野ではクリゾチニブおよびセリチニブのALK融合遺伝子検出は免疫組織染色がコンパニオン診断薬として認められています。しかし今のところ、ALK融合遺伝子以外で、研究用途を含めてキナーゼ融合遺伝子タンパク質を、効率よくかつ信頼性高く検出できる抗体はほとんどありません。例えばPan-TRK抗体の期待値は高いのですが、実際は当初報告されたよりも擬陽性が高いとも言われています。FISH法はTurn Around Timeが早いので結果が返ってくるまでが早いというメリットはありますが、ALK、RET、ROS1など各遺伝子ごとの検出となるため、効率は非常に悪いという欠点があります。PCRはマルチプレックスでデザインできますが、フュージョンパートナーがわかっていないと設計できないので、新規発見には向いていません。それらを比較して、新規発見の可能性があり、コスト面、ターゲット選択、プレックスの柔軟性や作業効率のメリットを考えると、NanoStringのnCounterによるimbalance解析は、融合遺伝子のスクリーニング手法として便利なので、活用させていただいています。
空間プロファイリングにより、腫瘍組織内のheterogeneityが治療の反応性に関わることがもし見つかれば、臨床的にも有用かもしれません。
―研究室でのご研究の中に、トリプルネガティブ乳がんにおけるTumor-infiltrating lymphocytesを探索したご研究があったかと思います。今後腫瘍周辺部位へのリンパ球浸潤度など、空間プロファイリングや空間オミクス解析が、診断や治療研究の分野に利用されていくでしょうか?
キナーゼ阻害剤は、奏功時の腫瘍縮小効果が目に見えて明らかですので、druggableな標的があるかないかを見つけるのに非常に有効です。アプローチの一つとして、私が今行っているimbalance解析では、できるだけ腫瘍部のみを含むようにダイゼクションして可能な限り腫瘍からのメッセージをとらえることが出来るように工夫していますが、腫瘍内のheterogeneityを今は全く観察出来ていません。しかし、キナーゼ阻害剤の使用後にもどうしてもきれいに縮小しない症例がありますので、腫瘍内の多様性が関係している可能性があるとは考えています。病理医は、形態変化や腫瘍組織像の変化に敏感で、腫瘍の分類や分化に関心が高いので、空間プロファイリングは有用なソリューションだと思います。
私自身は現在、治療標的となりうるような異常を見つけるといった治療に直結する研究を第一に考えていますが、空間プロファイリングにより、腫瘍組織内のheterogeneityが治療の反応性に大きく関わるというようなことがわかれば、臨床的にも非常に有用であるとも思います。治療前のバイオプシー検体と治療後の検体が残っていれば、治療奏功症例でそれらをレトロスペクティブな比較・解析することによって、バイオマーカー探索に利用できるかもしれません。

―今後の研究室、または先生個人のご研究目標などがありましたら、教えてください。
さまざまながん種での研究が進められていますが、がんを主軸に悪性度や患者個別の治療選択のための診断精度の向上を目的としての研究をこれからも進めていきたいと思っています。例えば、高悪性軟部肉腫でのGLI1遺伝子のコピー数異常を見たりするために、nCounterで腫瘍組織由来と非腫瘍由来のDNAをペアで解析することで遺伝子増幅をみることができるようなアッセイを組んだりしています。将来的に、遺伝子増幅の有無で治療の選択が変わってくるような発見ができればと、期待しています。境界に輪郭線を引き、それぞれの分画から情報を取るというようなGeoMx®のアプローチを活用させていただいています。
基礎科学よりも近い将来に治療に結び付くような研究でないと予算獲得が難しいという昨今の事情もありますが、研究計画を立てていくにあたり、、私はできるだけ治療に直結する、患者さんに還元できる臨床研究を念頭に置いています。また一方で、がんの発症メカニズムなどの基礎研究も必要だと思っていますので、基礎研究と治療に直結する仕事の二本柱で、今後も進めていくことになると思います。
-本日は誠にありがとうございました。
——————————————————————————————————————————————————-
注釈リンク
- Assessment of Predictive Biomarkers of the Response to Pazopanib Based on an Integrative Analysis of High-grade Soft-tissue Sarcomas. Clin Orthop Relat Res. 2021 Apr 1;479(4):838-852.
- Identification of a novel MAN1A1-ROS1 fusion gene through mRNA-based screening for tyrosine kinase gene aberrations in leiomyosarcoma. Clin Orthop Relat Res. 2021 Apr 1;479(4):838-852.
- nCounter Gene Fusion Panel.